(本文作者为 氨基观察,钛媒体经授权发布)
文 | 氨基观察
LAG-3 又塌房了。

3 月 13 日,Immutep 宣布,其可溶性 LAG-3 蛋白 efti 联合 K 药用于非小细胞肺癌一线治疗的Ⅲ期研究因疗效不佳提前终止,公司股价单日暴跌近 90%。
市场反应如此剧烈,原因在于这不仅是一项临床失败,更是一次预期崩塌。
单从靶点来看,LAG-3 并不算失败。至少,该靶点已诞生重磅药物。BMS 的 LAG-3/PD-1 双抗组合 Opdualag(Relatlimab+Nivolumab) 已在一线黑色素瘤适应症获批上市,2025 年其全球销售额达到 11.85 亿美元。
只是,免疫疗法的光环,注定这样的销售额远不足以满足市场期待。市场希望 LAG-3 能挺进更大的治疗领域。
也正因此,市场对 Immutep 在非小细胞肺癌领域的探索寄予厚望。
但随着此次临床项目宣告终止,市场不只是对 efti 感到失望,LAG-3 靶点的未来或许也需要重新审视。
/ 01 /Immutep 的“ 意外”
“ 鉴于 efti 在其他所有临床试验中的表现,我们对无效性分析的结果感到非常失望和惊讶。” 这是 Immutep 公司对该临床结果的表态,其实也是市场的一致性评价。
之所以感到意外,很大程度上在于 efti 此前的临床表现相当亮眼。
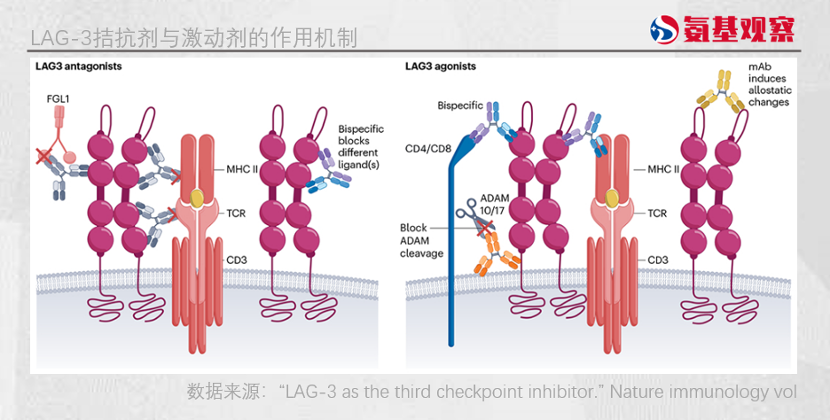
与传统的 LAG-3 抗体不同,efti 是一种可溶性 LAG-3 蛋白,通过与 MHCII 结合来主动激活抗原递呈细胞,从而增强 T 细胞免疫反应,理论上,这种机制能够放大抗肿瘤免疫应答。
这一机制差异也被认为可能绕开此前 LAG-3 抗体在实体瘤中的瓶颈,其早期临床数据表现也确实争气。
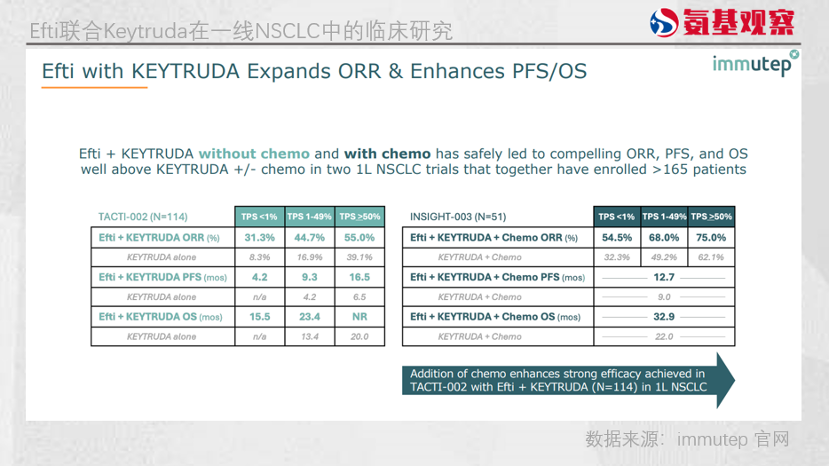
从 TACTI-002 试验中拆分的一组数据显示,efti 联合 K 药在未经治疗的不可切除或转移性 NSCLC 患者中取得了不错的疗效。在 114 名患者的治疗中,ORR 达到 40.4%,对比 K 药提升了近 1 倍。
更关键的是,该试验患者入组未按照 PD-L1 表达水平筛选,约 75% 的入组患者 PD-L1 评分低于 50%。对于 PD-L1 表达较低甚至阴性 (CPS<1) 的患者而言,这一结果显得尤为重要,因为这类患者通常难以从 PD-1 单药治疗中获益,一直被视为免疫治疗的相对空白人群。
在针对头颈鳞状细胞癌的 TACTI-003 研究中,efti 在 PD-L1 阴性患者的治疗潜力再次被验证。整体上,efti 联合 K 药组合 ORR 达到 32.8%,对比 K 药单药 26.7% 显著提高,而在 K 药不适用的阴性患者人群,联合用药 ORR 也达到了 26.9%。
在这样的背景下,关键性 TACTI-004 研究被寄予厚望。在合作方阿斯利康的协助下,临床试验推进速度也相当迅速。发布终止公告之前,756 名目标患者的入组进度已经过半。
可以说,TACTI-004 研究的预期被拉满了,但现实很残酷。
“ 根据对现有安全性和有效性数据的审查,独立数据监察委员会建议因试验无效而终止试验”。
TACTI-004 研究纳入的是 PD-L1 表达 0%—100% 的全人群患者,但在已入组半数的情况下仍建议终止试验,基本宣告 efti 一线治疗 NSCLC 已无可能。
尽管 NSCLC 受限,公司也并没有放弃该药,HR+/HER2-转移性乳腺癌和三阴性乳腺癌的 3 期临床仍在进行。但失去了肺癌这个肿瘤免疫治疗大市场,efti 的潜力受限。
更难以接受的是,市场对 efti 的疗效提出了质疑。GlobalData 的肿瘤和血液学分析师 BiswajitPodder 表示,在 NSCLC 试验中停止试验对 Immutep 来说是一个“ 重大挫折”。
/ 02 /走不出黑色素瘤
一度,LAG-3 被寄予厚望。
LAG-3 靶点早在 1990 年便已经被科学家发现,距离现在已经过去 30 年。这也使得,医学界对于 LAG-3 有了一些共识。
首先,LAG-3 作为一种免疫反应的负调节因子,它与抑制 T 细胞活化和细胞因子分泌有关,诱导免疫稳态; 因此,它有可能成为一个有前途的免疫检查点。
其次,LAG-3 表达已在多种类型的癌症中得到证实,即结直肠癌、胃癌、乳腺癌,甚至胰腺癌,这与它们的预后密切相关。这意味着,LAG-3 的应用范围比较广。
更重要的是,越来越多的临床前和临床证据强调了 LAG-3 阻断作为增强抗肿瘤免疫反应的可行策略的潜力,特别是 Opdualag 的成功获批证实了 LAG-3 和 PD-1 联合阻断能够带来治疗益处。
在上述逻辑下,市场一度对 LAG-3 充满期待。只是,截止目前,LAG-3 最成功的案例仍是黑色素瘤。
唯一获批药物 Opdualag 仅凭单一适应症,2025 年销售额达到了 11.85 亿美元。但自 2022 年获批以来,该药无新增适应症获批,甚至其针对黑色素瘤的辅助治疗的 3 期临床也没有达到主要终点。
一系列的临床失利,也让行业重新审视 LAG-3 是不是被高估了。
/ 03 /是不是被高估了?
事实上,从早期实验研究到临床实践都可以看到,LAG-3 单药疗效一般。
如 MC38 和 Sa1N 肿瘤小鼠模型中,LAG3 单药治疗效果甚微,仅能轻微抑制肿瘤生长,而肿瘤清除率极低。只有在与 PD-1 同时阻断时,才会出现一定程度的协同作用。
另一项临床试验分析了 PD-1 和/或 LAG-3 先导疗法在转移性黑色素瘤的表现,结果显示先导入 LAG-3,后引入 PD-1 抑制作用有限,反过来却生效。
显然 LAG-3 的定位更像是 PD-1 抑制剂的“ 搭档”,而不是单独驱动疗效的开关。
这也导致 LAG-3 的有效适应症比 PD-1 要窄得多。目前来看,其潜在优势可能集中在少数免疫敏感肿瘤,例如黑色素瘤、头颈癌以及部分乳腺癌亚型。但这部分患者当前靶向药选择药物竞争激烈,市场空间有限。
而在免疫治疗竞争最激烈的肺癌领域,上述临床结果已经证明,除非是特定的 PD-L1 高表达患者,否则 LAG-3 很难带来改善,更别提差异性的突破。
更深层的问题可能来自机制本身。
现有研究认为 LAG-3 的表达还受到多种酶的调控,其中金属蛋白酶 ADAM10 和 ADAM17 能够切割细胞表面的 LAG-3,使其以可溶形式脱落。这种动态变化使得 LAG-3 在不同肿瘤微环境中的表现不同,一些观点认为这会影响 LAG-3 在控制 T 细胞活化发挥的负调控作用。
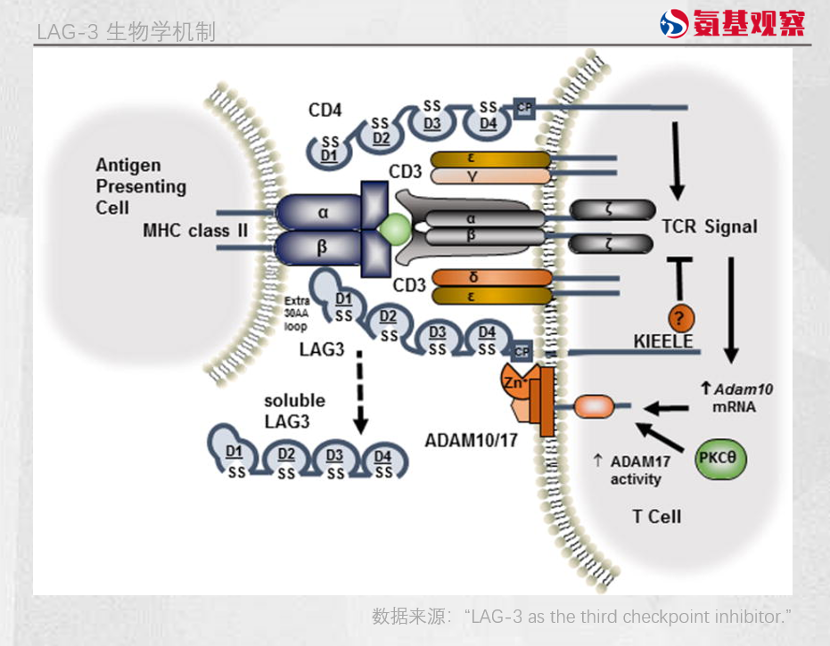
另一个关键问题则是 LAG-3 的配体,虽然 MHCII 类分子是 LAG-3 的核心配体,但其他配体在调节 LAG-3 表达后是否会激活进而影响抗癌作用有待进一步考量。
鉴于当前的理论基础以及临床表现,LAG-3 的市场预期,可能需要被重新审视。
/ 04 /总结
事实上,LAG-3 当前的处境其实并不孤立。
在 PD-1 之后,整个免疫治疗领域都在寻找“ 第二代免疫检查点”。无论是 LAG-3,还是 TIGIT、CTLA-4 都曾被寄予厚望,但现实是,这些 IO-2.0 靶点在多个关键适应症中推进得都不算顺利。
或许,这也在进一步提醒市场,无论是机制探索、药物设计,还是适应症选择,IO2.0 的探索的关键,还是要找到属于自己的最佳位置。
更多精彩内容,关注钛媒体微信号 (ID:taimeiti),或者下载钛媒体 App



